De ‘wet van Moore’ lijkt niet langer te gelden. Artificiële intelligentie verandert de manier waarop medicijnen ontwikkeld worden.
Vooruitgang in computing is lange tijd beschreven door de wet van Moore, een vuistregel die zegt dat de kosten van rekenkracht ongeveer elke twee jaar met de helft dalen. De farmaceutische industrie volgt een tegenovergestelde regel. Haar versie, de wet van Eroom (‘Moore’ achterstevoren gespeld), stelt dat de kosten voor de ontwikkeling van een nieuw medicijn ongeveer elke negen jaar verdubbelen. In de jaren zestig leverde 1 miljard dollar (tegen prijzen van 2008) aan onderzoek en ontwikkeling ongeveer tien nieuwe medicijnen op. Tegenwoordig is diezelfde 1 miljard dollar niet genoeg om er ook maar één te produceren.
Gemiddeld kost het nu tien jaar en meer dan 2 miljard dollar om een medicijn van begin tot eind te ontwikkelen. De risico’s zijn ook groot: minder dan een tiende van de kandidaat-geneesmiddelen die klinisch worden getest, wordt goedgekeurd door de regelgevende instanties. In de afgelopen tien jaar heeft de Amerikaanse Food and Drug Administration gemiddeld slechts 53 geneesmiddelen per jaar goedgekeurd. Voorstanders van artificiële intelligentie (AI) zeggen dat de technologie de potentie heeft om de ontwikkeling van medicijnen sneller en goedkoper te maken – iets wat zowel farmaceutische bedrijven als patiënten zouden verwelkomen. In 2025, wanneer een golf van nieuwe medicijnen de wettelijke goedkeuring nadert, zal AI die belofte beginnen in te lossen.
Nieuwe moleculen bedenken
De ontwikkeling van een geneesmiddel begint met het identificeren van een doelwit, zoals een eiwit of een gen, dat geassocieerd wordt met een bepaalde ziekte. Onderzoekers gaan dan op zoek naar een molecuul dat de activiteit van het doelwit kan blokkeren of versterken. Zodra potentiële moleculen zijn gevonden, worden ze getest op veiligheid en effectiviteit, eerst met behulp van computermodellen en daarna op dieren. Die fase, die bekend staat als de preklinische fase, kan het screenen van wel 1 miljoen verbindingen inhouden voordat er slechts één of twee veelbelovende kandidaten worden geselecteerd. Dat alles kan jaren duren en is goed voor bijna een derde van de ontwikkelingskosten van medicijnen, zelfs voordat ze op mensen worden getest.
Op AI gebaseerde methoden kunnen de productiviteit van onderzoek en ontwikkeling verdubbelen.
In die preklinische fase gebruiken geneesmiddelenproducenten AI om hun kansen te vergroten. De farmaceutische industrie gebruikt al tientallen jaren computermodellen, maar AI verandert de ontdekking van medicijnen op verschillende manieren. Ten eerste verbetert AI het inzicht van onderzoekers in ziekten en hun doelwitten door enorme hoeveelheden gegevens te analyseren. Software kan ook veelbelovende moleculen en hun structuur verfijnen om het succes bij proeven op mensen te vergroten. Generatieve AI kan nog een stap verder gaan door geheel nieuwe moleculen te bedenken om te testen.
In 2020 verbaasde AlphaFold 2, een model gemaakt door DeepMind, een AI-laboratorium dat eigendom is van Google, de wetenschappelijke wereld door nauwkeurig de structuur van bijna elk eiwit in het menselijke lichaam te voorspellen. In mei 2024 breidde zijn opvolger, AlphaFold 3, zijn mogelijkheden uit naar andere moleculen waaruit levende wezens bestaan: eiwitten, DNA, RNA en kleine moleculen die liganden worden genoemd. Zulke modellen veranderen de ontwikkeling van medicijnen door maanden van trial-and-errorexperimenten terug te brengen tot slechts enkele uren rekenwerk. Insilico, een start-up die AI gebruikt om medicijnen te ontwikkelen, zegt dat zijn software een nieuw doelwit voor medicijnen heeft geïdentificeerd en een molecuul heeft ontworpen dat geschikt is voor proeven op mensen in slechts achttien maanden, tegen een prijs van 2,7 miljoen dollar – een fractie van de gebruikelijke tijd en kosten.
Eczeem en kanker
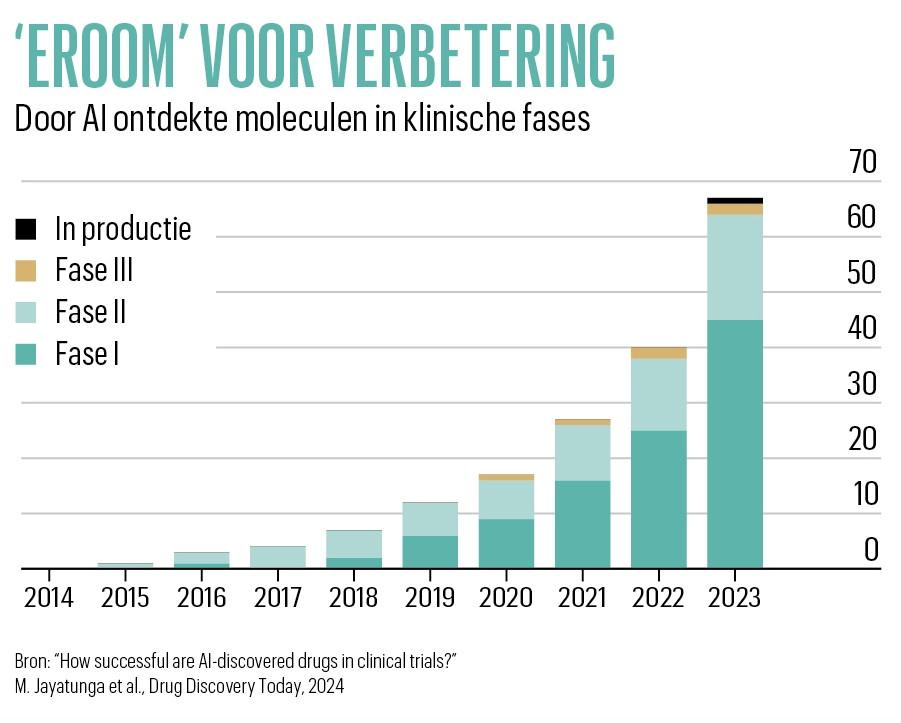
Doorbraken in de preklinische fase zijn doorgedrongen tot de zakelijke kant van de medicijnontwikkeling. Het adviesbureau BCG schat dat er ongeveer 65 AI-geïnspireerde moleculen worden getest op mensen (zie grafiek). Ongeveer een derde daarvan bevindt zich in de tweede fase van het klinisch onderzoek, waarin het medicijn wordt getest op effectiviteit en bijwerkingen. Bedrijven moeten dan beslissen of ze doorgaan met de duurdere fase III-studies op een grotere populatie. Minder dan een derde van de kandidaat-geneesmiddelen maakt die sprong.
In 2025 zullen de resultaten van de cruciale tweede fase worden gerapporteerd voor meer dan een half dozijn geneesmiddelen. Sommige door AI ontworpen medicijnen zijn in die fase al gestruikeld. BenevolentAI en Exscientia, twee veelbelovende Britse AI-start-ups, rapporteerden onlangs teleurstellende resultaten in klinische onderzoeken voor hun geneesmiddelen tegen eczeem en kanker. Ondanks die tegenslagen gelooft Christoph Meier van BCG dat op AI gebaseerde methoden de productiviteit van onderzoek en ontwikkeling kunnen verdubbelen. En het lijkt waarschijnlijk dat vier of vijf door AI ontwikkelde behandelingen, zo niet meer, in 2025 door kunnen gaan naar proeven in fase drie.
Dit is een kleine steekproef, maar die medicijnen wijzen op een ingrijpende verandering in de ontwikkeling van medicijnen. Hoewel AI de tijdschema’s voor klinische tests nog niet heeft verkort, helpt het farmaceutische bedrijven al slimmere keuzes te maken over welke moleculen ze verder willen ontwikkelen, waardoor het aantal mislukkingen afneemt en de kosten dalen. Uit onderzoek van Andreas Bender aan de Universiteit van Cambridge blijkt bijvoorbeeld dat het terugdringen van het aantal mislukkingen in fase II-onderzoeken met slechts 20 procent een besparing van bijna 450 miljoen dollar kan opleveren voor de ontwikkeling van één geneesmiddel. In de computerwereld is de wet van Moore op zijn retour. In de farmaceutische industrie zou de wet van Eroom binnenkort weleens hetzelfde lot kunnen ondergaan.





